| Amonia | |
|---|---|
 | |
| Tổng quan | |
| Danh pháp IUPAC | Ammonia Azane |
| Tên khác | Azane |
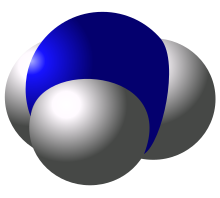
| Công thức phân tử | NH3 |
| Phân tử gam | 17,02982 g/mol |
| Biểu hiện | Chất khí ko màu mùi khai |
| Số CAS | [7664-41-7] |
| Thuộc tính | |
| Tỷ trọng và pha | 0,6813 g/l, khí |
| Độ hòa tan nhập nước | 89,9 g/100 ml ở 0 ℃ |
| Nhiệt nhiệt độ chảy | −77,73 °C (−107,91 °F; 195,42 K) |
| Điểm sôi | −33,34 °C (−28,01 °F; 239,81 K) |
| pKa | ≈ 34 |
| pKb | 4,75 |
| Khác | |
| MSDS | MSDS ngoài |
| Các nguy nan chính | Chất bào mòn và hóa học độc |
| NFPA 704 | |
| Điểm bắt lửa | 11 ℃ |
| Rủi ro/An toàn | R10, R23, R34, R50 S1/2, S16, S36/37/39, S45, S61 |
| Số RTECS | BO0875000 |
| Các ăn ý hóa học liên quan | |
| Các ăn ý hóa học liên quan | Hiđrazin Axit hydrazoic Hydroxylamin Cloramin |
| Ngoại trừ với thông tin không giống, những dữ liệu được lấy ở 25 °C, 100 kPa Thông tin cẩn về sự việc không đồng ý và tham lam chiếu | |
Amonia (bắt mối cung cấp kể từ từ giờ đồng hồ Pháp ammoniac /amɔnjak/),[1] còn được ghi chép là a-mô-ni-ắc,[1] là một trong những ăn ý hóa học của nitơ và hydro với công thức chất hóa học NH3. Là một hydride nhị phân ổn định quyết định và hydride pnictogen giản dị nhất, amonia là một trong những hóa học khí ko màu sắc, với mùi khó chịu đặc thù (mùi khai). Nó là một trong những hóa học thải nitơ thịnh hành, nhất là trong những loại vật sinh sống bên dưới nước, và nó thêm phần đáng chú ý nhập nhu yếu đủ chất của những loại vật bên trên cạn bằng phương pháp nhập vai trò là chi phí hóa học của đồ ăn và phân bón. Thanh, thẳng hoặc loại gián tiếp, cũng là một trong những hóa học xây cất nhằm tổ hợp nhiều thành phầm dược phẩm và được dùng trong tương đối nhiều thành phầm tẩy cọ thương nghiệp. Nó hầu hết được tích lũy bằng phương pháp tổ hợp hạ nút của không gian và nước.
Bạn đang xem: nh3 là axit hay bazơ
Mặc cho dù khá thịnh hành nhập đương nhiên – cả bên trên cạn và ở những hành tinh anh phía bên ngoài Hệ Mặt trời - và được dùng rộng thoải mái, amonia vừa phải với tính bào mòn vừa phải nguy nan ở dạng đậm quánh. Nó được phân loại là một trong những hóa học khôn cùng nguy nan ở Hoa Kỳ và cần tuân bám theo những đòi hỏi report nghiêm nhặt bởi vì những hạ tầng phát hành, tàng trữ hoặc dùng nó với lượng đáng chú ý.[2]
Sản lượng amonia công nghiệp toàn thế giới năm 2018 là 175 triệu tấn,[3] không tồn tại thay cho thay đổi đáng chú ý đối với sản lượng công nghiệp toàn thế giới năm trước đó là 175 triệu tấn.[4] Amonia công nghiệp được cung cấp bên dưới dạng rượu amonia (thường là 28% amonia nhập nước) hoặc amonia lỏng khan với áp suất hoặc thực hiện giá buốt được vận fake nhập xe pháo bể hoặc ống trụ.[5]
NH3 sôi ở -33,34 ℃ ở áp suất chi phí chuẩn chỉnh, bởi vậy hóa học lỏng cần được bảo vệ bên dưới áp suất hoặc ở sức nóng chừng thấp. Amonia gia dụng hoặc amoni hydroxide là một trong những hỗn hợp NH3 nội địa. Nồng chừng của những hỗn hợp này được đo bởi vì đơn vị chức năng của thang Baumé (khối lượng riêng), với 26 chừng Baumé (khoảng 30% (theo trọng lượng) amonia ở 15,5 °C hoặc 59,9 °F) là thành phầm thương nghiệp mật độ cao nổi bật của hóa học này.[6]
Từ nguyên[sửa | sửa mã nguồn]
Pliny, nhập Sách XXXI về Lịch sử Tự nhiên của tôi, nói đến một loại muối hạt được phát hành ở tỉnh Cyrenaica của La Mã mang tên là hammoniacum, được gọi như thế vì như thế nó ở ngay sát Đền thờ Jupiter Amun (tiếng Hy Lạp là Ἄμμων Ammon).[7] Tuy nhiên, tế bào mô tả của Pliny về muối hạt ko phù phù hợp với những đặc điểm của amoni chloride. Theo điều comment của Herbert Hoover nhập phiên bản dịch giờ đồng hồ Anh của ông về De re metallica của Georgius Agricola, nó rất có thể là muối hạt hải dương thường thì.[8] Trong từng tình huống, muối hạt bại liệt sau cùng đang được đưa đến thương hiệu cho những ăn ý hóa học amonia và amoni.
Xuất hiện tại nhập tự động nhiên[sửa | sửa mã nguồn]
Amonia là một trong những Hóa chất được nhìn thấy ở dạng vi lượng nhập đương nhiên, được phát hành kể từ hóa học động thực vật với nitơ. Amonia và muối hạt amoni cũng khá được nhìn thấy với con số nhỏ nội địa mưa, trong những khi amoni chloride (sal amonia), và amoni sulfat được nhìn thấy ở những vùng với núi lửa; tinh anh thể Amoni bicarbonat đã và đang được nhìn thấy nhập phân chim Patagonia.[9] Thận tiết đi ra amonia nhằm dung hòa acid dư quá.[10] Các muối hạt amoni được nhìn thấy trong số vùng khu đất phì nhiêu và nội địa hải dương.
Amonia cũng khá được nhìn thấy bên trên từng những hành tinh anh nhập hệ Mặt Trời bên trên sao Hỏa, sao Mộc, sao Thổ, sao Thiên Vương, sao Hải Vương, và Sao Diêm Vương, và những điểm khác: bên trên, bên trên những hành tinh anh nhỏ hơn hoàn toàn như là Sao Diêm Vương, amonia rất có thể hoạt động và sinh hoạt như 1 hóa học chống sầm uất mang ý nghĩa địa hóa học cần thiết, vì thế lếu ăn ý của nước và amonia rất có thể với sức nóng nhiệt độ chảy thấp cho tới 173 K (−100 °C; −148 °F) nếu như mật độ amonia đầy đủ cao và bởi vậy được cho phép những thiên thể như thế tích lại những hồ nước bên phía trong và địa hóa học đang được hoạt động và sinh hoạt ở sức nóng chừng thấp rất là nhiều đối với tình huống hành tinh anh chỉ mất nước.[11][12] Các hóa học với chứa chấp amonia, hoặc những hóa học tương tự động với nó, được gọi là amoniaal.
Tính hóa học vật lý[sửa | sửa mã nguồn]
Amonia là hóa học khí ko màu sắc, với hương thơm hắc đặc thù. Nó nhẹ nhàng rộng lớn không gian, tỷ lệ của chính nó cấp 0,589 lượt không gian. Nó đơn giản hóa lỏng vì thế với link hydro mạnh trong những phân tử; hóa học lỏng sôi ở −33,3 °C (−27,94 °F), và ngừng hoạt động trở thành tinh anh thể white [9] ở −77,7 °C (−107,86 °F).
Amonia rất có thể được khử hương thơm thuận tiện bằng phương pháp mang lại nó phản xạ với natri bicacbonat hoặc axit axetic. Cả nhì phản xạ này đều tạo ra trở thành muối hạt amoni ko hương thơm.
- Chất rắn
Đối xứng tinh anh thể là hình khối, ký hiệu Pearson cP16, group không khí P213 (№. 198), hằng số mạng 0,5125 nm.
- Chất lỏng
Amonia dạng lỏng với năng lực ion hóa mạnh vì thế với chỉ số ε cao là 22. Amonia lỏng với sự thay cho thay đổi entanpi của quy trình hóa khá chi phí chuẩn chỉnh vô cùng cao (23,35 kJ/mol, cf. nước 40,65 kJ/mol, methan 8,19 kJ/mol, photphin 14,6 kJ/mol) và bởi vậy rất có thể được dùng nhập chống thử nghiệm trong số bình ko chống nóng tuy nhiên ko cần thiết thực hiện giá buốt thêm thắt. Xem amonia lỏng như 1 dung môi.
- Thuộc tính dung môi
Amonia đơn giản hòa tan nội địa. Trong hỗn hợp nước, nó rất có thể được vô hiệu hóa bằng phương pháp hâm nóng. Dung dịch nước của amonia với tính base. Nồng chừng tối nhiều của amonia nội địa (dung dịch bão hòa) với lượng riêng rẽ là 0,880 g/cm³ và thông thường được gọi là '880 amonia'.
- Cháy
Amonia ko cháy tức thì hoặc với năng lực lưu giữ sự cháy, nước ngoài trừ nhập ĐK lếu ăn ý nhiên liệu-không khí hẹp với 15–25% không gian. Khi trộn với oxy, nó cháy với ngọn lửa gold color lục nhạt nhẽo. Sự bốc cháy xẩy ra Lúc clo được truyền nhập amonia, tạo ra trở thành nitơ và hydro chloride; nếu như clo dư thì nitơ trichloride (NCl3) rất đơn giản nổ cũng khá được tạo ra trở thành.
- Sự phân hủy
Ở sức nóng chừng cao và xuất hiện hóa học xúc tác tương thích, amonia bị phân bỏ trở thành những yếu tắc cấu trở thành của chính nó. Sự phân bỏ amonia là một trong những quy trình thu sức nóng nhẹ nhàng cần thiết 5,5 kcal/mol amonia, và đưa đến khí hydro và nitơ. Amonia cũng rất có thể được dùng như 1 mối cung cấp hydro mang lại pin nhiên liệu axit nếu như amonia ko phản xạ rất có thể được vô hiệu hóa. Các hóa học xúc tác ruthenium và platinum được cho rằng hoạt động và sinh hoạt tích vô cùng nhất, trong những khi những hóa học xúc tác Ni được tương hỗ thì hoạt động và sinh hoạt xoàng xĩnh rộng lớn.
Cấu trúc[sửa | sửa mã nguồn]
Phân tử amonia với hình trạng chóp tam giác bám theo Dự kiến của thuyết đẩy cặp electron lớp vỏ hóa trị (thuyết VSEPR) với góc link xác lập bởi vì thực nghiệm là 106,7°.[13] Nguyên tử nitơ trung tâm với năm electron lớp bên ngoài cùng theo với một electron bổ sung cập nhật kể từ từng vẹn toàn tử hydro. Vấn đề này đưa đến tổng số tám năng lượng điện tử, hoặc tứ cặp năng lượng điện tử được bố trí theo như hình tứ diện. Ba nhập số những cặp electron này được dùng tựa như các cặp link, bọn chúng nhằm lại một cặp electron có một không hai. Cặp đơn lẻ tăng nhanh rộng lớn những cặp link, bởi vậy góc link ko cần là 109,5°, như mong ngóng so với bố trí tứ diện đều, tuy nhiên là 106,7°.[13] Hình dạng này tạo ra mang lại phân tử một momen lưỡng vô cùng và thực hiện mang lại nó phân vô cùng. Tính phân vô cùng của phân tử, và quan trọng, năng lực tạo hình link hydro của chính nó, thực hiện mang lại amonia rất có thể trộn lộn với nước vô cùng cao. Cặp đơn độc thực hiện mang lại amonia phát triển thành một base, một hóa học nhận proton. Amonia với tính base vừa phải phải; Dung dịch nước 1,0 M với pH là 11,6, và nếu như thêm thắt axit mạnh nhập hỗn hợp như thế cho tới Lúc hỗn hợp trung tính (pH = 7), 99,4% số phân tử amonia được proton hóa. Nhiệt chừng và chừng đậm cũng tác động cho tới tỷ trọng NH4+. Sau này còn có hình dạng của một tứ diện đều và là đẳng năng lượng điện tử với methan.
Phân tử amonia đơn giản trải qua loa quy trình nghịch ngợm fake nitơ ở sức nóng chừng phòng; một luật lệ tương tự động hữu ích là một trong những cái dù tự động tảo ra phía bên ngoài nhập một cơn gió máy mạnh. Rào cản tích điện so với sự nghịch ngợm hòn đảo này là 24,7 kJ/mol và tần số nằm trong hưởng trọn là 23,79 GHz, ứng với sự phản xạ vi sóng với bước sóng 1,260 cm. Sự hít vào ở tần số này là phổ vi sóng thứ nhất được để ý thấy.
Tính lưỡng tính[sửa | sửa mã nguồn]
Một trong mỗi đặc thù đặc thù nhất của amonia là tính base. Amonia được xem là một base yếu đuối. Nó kết phù hợp với axit sẽ tạo trở thành muối; bởi vậy với axit clohydric nó tạo ra trở thành amoni chloride (sal amonia); với axit nitric tạo ra trở thành amoni nitrat, v.v. Amonia thô trọn vẹn sẽ không còn kết phù hợp với hydro chloride thô trả toàn; nhiệt độ là quan trọng nhằm triển khai phản xạ. [14][15] Như một thử nghiệm tế bào mô tả, những chai amonia và axit clohydric đậm quánh đang được há nắp đưa đến những "đám mây" amoni chloride, nhượng bộ như xuất hiện tại kể từ "không với gì" Lúc muối hạt tạo hình điểm nhì đám mây phân tử khuếch giã bắt gặp nhau, ở nơi nào đó thân thuộc nhì chai.
NH3 + HCl → NH4Cl
Các muối hạt được đưa đến vì thế tính năng của amonia với axit được gọi là muối hạt amoni và toàn bộ đều chứa chấp ion amoni (NH4+). Mặc cho dù amonia được nghe biết là một trong những base yếu đuối, nó cũng rất có thể hoạt động và sinh hoạt như 1 axit khôn cùng yếu đuối. Nó là một trong những hóa học proton và với năng lực tạo hình amit (có chứa chấp ion NH2−). Ví dụ, lithi hòa tan nhập amonia lỏng sẽ tạo đi ra hỗn hợp lithi amit:
2Li + 2NH3 → 2LiNH2 + H2
Tính hóa học hóa học[sửa | sửa mã nguồn]
Trong amonia, nitơ với số lão hóa thấp nhất nên amonia với tính khử. Ví dụ như nhập phản xạ hóa học:
Nguyên tử sắt kẽm kim loại loại kiềm hoặc nhôm:
Xem thêm: điểm chuẩn đại học nha trang 2022
Tác dụng với hỗn hợp muối:
Tính base yếu[sửa | sửa mã nguồn]
Tan nhập nước[sửa | sửa mã nguồn]
Theo thuyết Brønsted-Lowry, NH3 Lúc tan nội địa, 1 phần nhỏ những phân tử amonia kết phù hợp với ion H+ của nước tạo ra trở thành cation amoni NH4+ và giải hòa anion OH-, thời điểm này nước tiếp tục nhập vai trò là axit.
- \]
Ion OH- thực hiện mang lại hỗn hợp với tính base, tuy vậy đối với hỗn hợp kiềm mạnh (thí dụ xút, potat, nước vôi nhập...) nằm trong mật độ thì mật độ anion OH- vì thế amonia tạo ra trở thành nhỏ rất là nhiều. Do với tính base nên hỗn hợp amonia thực hiện mang lại quỳ tím hóa xanh rì còn hỗn hợp phenolphtalein kể từ ko màu sắc fake trở thành hồng. Do bại liệt nhằm trừng trị hiện tại amonia, người tao sử dụng quỳ tím độ ẩm nhằm quan sát khí này.
Tác dụng với axit[sửa | sửa mã nguồn]

Amonia (ở dạng khí tương tự dung dịch) đơn giản dung hòa axit tạo ra trở thành muối hạt amoni. Thí dụ:
hay
Khi bịa nhì bình há nút đựng hỗn hợp HCl quánh và hỗn hợp NH3 ở ngay sát nhau thì thấy với "khói" white color tạo thành (hình 1). Do HCl và NH3 là những ăn ý hóa học dễ dàng cất cánh khá nên bọn chúng đang được hóa phù hợp với nhau tạo ra trở thành tinh anh thể muối hạt amoni chloride, chủ yếu tinh anh thể này đang được tạo thành hiện tượng lạ "khói".
Phản ứng này được dùng để làm phân biệt khí amonia.
Tác dụng với hỗn hợp muối[sửa | sửa mã nguồn]

Dung dịch amonia với năng lực tạo ra kết tủa nhiều hydroxide sắt kẽm kim loại Lúc tác dụng
Thí dụ nhập hình 2, hỗn hợp amonia đang được phản xạ với hỗn hợp đồng(II) sunfat tạo ra kết tủa xanh rì lam:
Khả năng tạo ra phức[sửa | sửa mã nguồn]
Dung dịch amonia với năng lực tạo ra phức với thật nhiều ăn ý hóa học khó khăn tan của sắt kẽm kim loại như Cu, Ag, Ni, Pb, Zn,…
Vì những cation này còn có orbital trống không nên rất có thể tiêu thụ cặp electron ko link nhập vẹn toàn tử N của NH3.
- (với M = Cu, Zn, Pb,…)
Điều chế[sửa | sửa mã nguồn]
Trong chống thí nghiệm:
Trong công nghiệp:
Phần rộng lớn NH3 (90%) được phát hành bám theo công thức Haber-Bosch với kể từ không gian, kể từ khí Mêtan () và nước.
- (xúc tác Ni, sức nóng chừng cao)
(ΔH = –92 kJ/mol)
Phản ứng bên trên thuận nghịch ngợm và lan sức nóng, bởi vậy cần với những ĐK thích hợp nhằm di chuyển cân đối về phía bên phải bám theo nguyên tắc Le Chatelier. Thực tế, phản xạ này thông thường được triển khai ở 450–500 ℃, 200–300 atm, xúc tác là lếu ăn ý Fe, Al2O3, K2O,… tuy nhiên hiệu suất chỉ với 20–25%. Phương thức CaCN2 của Rothe-Frank-Caro:
Phương thức Persek kể từ nhôm nitride AlN và nước:
Từ NO và H2:
Khử hydro bởi vì nitơ (tiếng anh: hydrodenitrogenation)
Xem thêm: hôm nay là thứ bảy
Hiện ni, một vài nghiên cứu và phân tích kể từ chống thử nghiệm đã cho chúng ta thấy rằng ammonia được phát hành thẳng kể từ nitơ và nước với việc xuất hiện của hóa học xúc tác titan(IV) oxide và tia vô cùng tím:
Ứng dụng[sửa | sửa mã nguồn]
Ứng dụng hầu hết của amonia là vấn đề chế phân đạm, pha trộn axit nitric, là hóa học sinh hàn, phát hành hiđrazin N2H4 dùng để nhiên liệu mang lại thương hiệu lửa. Hình như, hỗn hợp amonia còn được sử dụng thực hiện hóa học tẩy cọ gia dụng.
Nguy hiểm[sửa | sửa mã nguồn]
Nếu hít nhiều amonia có khả năng sẽ bị phỏng đàng thở (rát cổ họng). Khí amonia làm cho khắc chế thần kinh trung ương tạo thành cảm xúc không dễ chịu gắt gắt. Triệu chứng: Ho, nhức ngực (nặng), nhức thắt ngực, nghẹt thở, thở thời gian nhanh, thở khò khè, nghẹt thở, ho đi ra huyết, teo lắc với những biểu hiện:
- Mắt, mồm, họng: Chảy nước đôi mắt và châm đôi mắt, loà đôi mắt, rát họng nặng nề, miệng gặp vấn đề đau, sứt mẻ môi .
- Tim mạch: Nhanh, mạch yếu đuối, sốc.
- Thần kinh: Lẫn lộn, đi đi lại lại trở ngại, đau đầu và chóng mặt, thiếu thốn sự kết hợp, thấp thỏm, ngơ ngẩn.
- Da: Môi xanh rì lợt màu sắc, phỏng nặng nề nếu như xúc tiếp lâu.
- Dạ dày và đàng chi phí hóa: Đau bao tử nghiệm trọng, ọe.
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d’origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 49.
- ^ “40 C.F.R.: Appendix A vĩ đại Part 355—The List of Extremely Hazardous Substances and Their Threshold Planning Quantities” (PDF) . Government Printing Office. Bản gốc (PDF) tàng trữ ngày 25 mon hai năm 2012. Truy cập ngày 29 mon 10 năm 2011.
- ^ “Mineral Commodity Summaries 2020, p. 117 – Nitrogen” (PDF). USGS. 2020. Truy cập ngày 12 mon hai năm 2020.
- ^ “Nitrogen (fixed) - ammonia statistics”. USGS. 2017. Truy cập ngày 12 mon hai năm 2020.
- ^ R. Norris Shreve; Joseph Brink (1977). Chemical Process Industries (ấn phiên bản 4). tr. 276. ISBN 978-0-07-057145-7. See also Gas carrier and Bottled gas.
- ^ “Ammonium hydroxide physical properties” (PDF). Bản gốc (PDF) tàng trữ ngày 27 mon 11 trong năm 2007.
- ^ “Pliny the Elder, The Natural History, Book XXXI, Chapter 39. (7.) - The various kinds of salt; the methods of preparing it, and the remedies derived from it”.
- ^ Hoover, Herbert (1950). Georgius Agricola De Re Metallica - Translated from the first Latin edition of 1556. New York: Dover Publications. tr. 560. ISBN 978-0486600062.
- ^ a b Chisholm 1911, tr. 861.
- ^ Kirschbaum, B; Sica, D; Anderson, F. P.. (1999). “Urine electrolytes and the urine anion and osmolar gaps”. The Journal of Laboratory and Clinical Medicine. 133 (6): 597–604. doi:10.1016/S0022-2143(99)90190-7. ISSN 0022-2143. PMID 10360635.
- ^ Shannon, Francis Patrick (1938) Tables of the properties of aqua-ammonia solutions. Part 1 of The Thermodynamics of Absorption Refrigeration. Lehigh University studies. Science and technology series
- ^ An ammonia-water slurry may swirl below Pluto's icy surface. Purdue University (ngày 9 mon 11 năm 2015)
- ^ a b Haynes, William M. chỉnh sửa (2013). CRC Handbook of Chemistry and Physics (ấn phiên bản 94). CRC Press. tr. 9–26. ISBN 9781466571143.
- ^ Chisholm 1911, tr. 862.
- ^ Baker, H. B. (1894). “Influence of moisture on chemical change”. J. Chem. Soc. 65: 611–624. doi:10.1039/CT8946500611.
- Hóa học tập vô sinh, tập dượt nhì, Hoàng Nhâm, Nhà xuất phiên bản dạy dỗ nước Việt Nam.
- Sách giáo khoa Hóa học tập 11 nâng lên, Nhà xuất phiên bản dạy dỗ nước Việt Nam.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons được thêm hình hình họa và phương tiện đi lại truyền đạt về Amonia. |
- AMONIAC bên trên Từ điển bách khoa Việt Nam
- Ammonia (chemical compound) bên trên Encyclopædia Britannica (tiếng Anh)
- CID 222 kể từ PubChem

![{\displaystyle {\ce {4NH3 + 3O2 ->[500^o C] 2N2 + 6H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/24713424b16a6d0cb2f68374c1c5a0f360121f09)
![{\displaystyle {\ce {2NH3 + 2Na ->[350^o C] 2NaNH2 + H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e34b4c906c4f4889ec830f56054d37a9e6363060)
![{\displaystyle {\ce {2NH3 + 2Al ->[800-900^o C] 2AlN + 3H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/375054d38ad80d520769fdc6ebd0e7cf606f25bd)






2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/161640ee3e29c23b3c2fc7c5db961cfa230f0cc4)
2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9db405cbec65824bb3a148c735155fbc976329b4)
![{\displaystyle {\ce {Ag+ + 2NH3 -> [Ag(NH3)2]+}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6a54fcb6a7a78659b60e2e2e3fccb837b0a11a7c)











![{\displaystyle {\xrightarrow[{\text{UV}}]{{\text{TiO}}_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/19eca1eae28c21ed403c989342041b52e35d1ba6)












Bình luận